IGF2BP3 promotes progression of head and neck cancers through the circHECTD2/
hsa_miR_4310/7157-5p/Smad2 signaling axis in an m6 A modification–dependent manner
(IF=33.8990) 《Molecular Cancer》
摘要
头颈部鳞状细胞癌(HNSCC)发病率高、易侵袭转移、预后差,其分子机制尚未完全阐明。N6甲基腺苷(m⁶A)修饰与环状RNA(circRNA)在肿瘤中发挥关键调控作用,但二者协同调控HNSCC进展的机制仍不明确。
本研究发现,m⁶A阅读蛋白IGF2BP3在HNSCC中显著高表达,且与患者不良预后密切相关。机制上,IGF2BP3通过KH3结构域结合METTL3介导m⁶A修饰的circHECTD2,增强其稳定性。
circHECTD2作为内源竞争RNA(ceRNA)吸附miR4310和miR71575p,解除其对SMAD2的抑制,进而激活TGFβ通路,促进HNSCC增殖、侵袭与转移。
本研究阐明了IGF2BP3/circHECTD2/miR4310/71575p/SMAD2调控轴在HNSCC中的促癌机制,为HNSCC提供了新的预后标志物与潜在治疗靶点。
一、引言
头颈部鳞状细胞癌(HNSCC)是全球第七大恶性肿瘤,具有局部侵袭性强、易淋巴结转移、5年生存率不足50%等特点。
尽管手术、放化疗及靶向治疗不断进步,HNSCC复发与转移仍是治疗失败的主要原因,因此亟需揭示其恶性进展的分子机制,寻找新的诊断与治疗靶点。
环状RNA(circRNA)由反向剪接形成闭合环状结构,稳定性高、组织特异性强,可通过ceRNA机制吸附microRNA(miRNA)调控靶基因表达,广泛参与肿瘤发生发展。
m⁶A是真核生物mRNA与非编码RNA最丰富的表观修饰,由甲基转移酶(writer)、去甲基酶(eraser)、阅读蛋白(reader) 动态调控,影响RNA的剪接、稳定、翻译与定位。
IGF2BP3作为重要的m⁶A阅读蛋白,可结合m⁶A位点增强靶RNA稳定性,在多种肿瘤中发挥促癌作用,但其在HNSCC中调控circRNA的机制尚未报道。
本研究以m⁶A修饰circRNAceRNA调控轴为核心,系统探究IGF2BP3在HNSCC中的功能与分子机制,明确其下游circHECTD2、miR4310/71575p及SMAD2的调控关系,为HNSCC的靶向治疗提供理论依据。
二、材料与方法
2.1 临床组织样本收集
山东大学齐鲁医院120例HNSCC患者癌组织及配对癌旁组织,所有患者均经病理确诊,术前未接受放化疗,研究经伦理委员会批准。
2.2 细胞系与培养
HNSCC细胞系FaDu、Tu686、SCC9培养于含10%胎牛血清的DMEM/DMEM/F12培养基,37℃、5% CO₂条件下培养。
2.3 质粒构建与细胞转染
构建IGF2BP3、circHECTD2、SMAD2过表达载体及shRNA/siRNA干扰载体;采用慢病毒包装建立稳定敲低/过表达细胞株,转染试剂为jetPRIME。
2.4 RNA与蛋白检测
qRTPCR检测RNA表达;Western blot检测IGF2BP3、SMAD2、pSMAD2等蛋白水平;免疫组化(IHC)、RNA原位杂交(RNAISH)检测组织中分子表达。
2.5 分子互作实验
RNA免疫沉淀(RIP)、m⁶A甲基化RNA免疫沉淀(MeRIP)、RNA pulldown、RNA反义纯化(RAP)、电泳迁移率实验(EMSA)、双荧光素酶报告实验验证分子结合与调控。
2.6 细胞功能实验
CCK8、EdU、克隆形成实验检测细胞增殖;Transwell、划痕实验检测迁移与侵袭。
2.7 动物实验
BALB/c裸鼠皮下成瘤实验检测体内增殖;尾静脉注射构建肺转移模型,评估转移能力。
2.8 生物信息学与统计学分析
TCGA数据库、单细胞测序筛选差异基因;miRanda、RNAhybrid预测miRNA靶点;SPSS、GraphPad Prism进行统计分析,P<0.05为差异具有统计学意义。
三、结果
3.1 IGF2BP3在HNSCC中高表达并提示不良预后
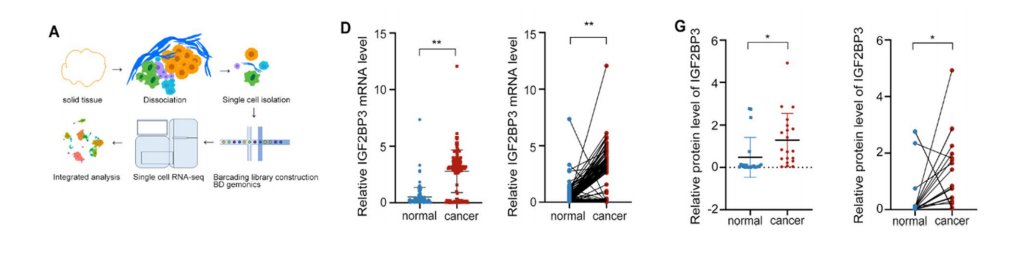
• TCGA数据分析、单细胞测序、qRTPCR、Western blot及IHC显示,IGF2BP3在HNSCC组织与细胞中显著高表达。
• 生存分析表明,IGF2BP3高表达患者总生存期显著缩短,且与肿瘤大小、饮酒史、T分期密切相关。
• 体外敲低IGF2BP3可显著抑制HNSCC细胞增殖、迁移与侵袭;过表达则增强上述恶性表型。
• 裸鼠实验证实,IGF2BP3敲低抑制皮下成瘤与肺转移,过表达则促进肿瘤生长与转移。
3.2 鉴定并验证IGF2BP3的下游靶标circHECTD2
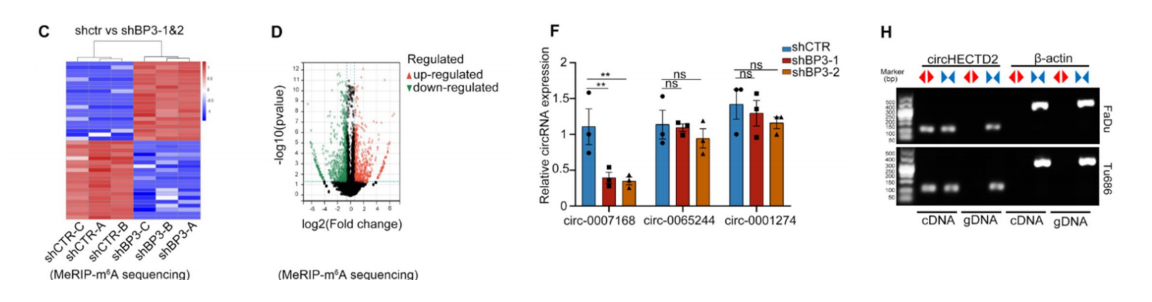
• circRNA测序与m⁶AMeRIP测序联合分析,筛选出IGF2BP3调控的候选circRNA,确定circHECTD2(hsa_circ_0007168)为关键靶标。
• circHECTD2由HECTD2基因外显子25反向剪接形成,长度462 nt,主要定位于细胞质,稳定性显著高于线性mRNA。
• circHECTD2在HNSCC组织中高表达,与IGF2BP3表达呈正相关,高表达患者预后更差。
• 敲低circHECTD2可抑制HNSCC细胞增殖、侵袭与体内成瘤及转移,过表达则促进恶性表型。
3.3 IGF2BP3通过m⁶A修饰稳定circHECTD2
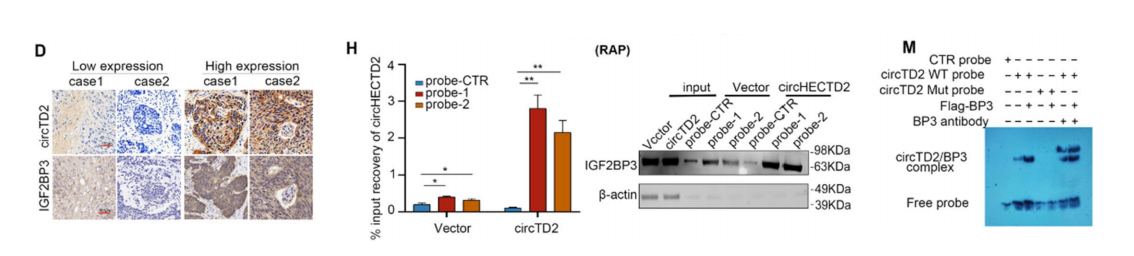
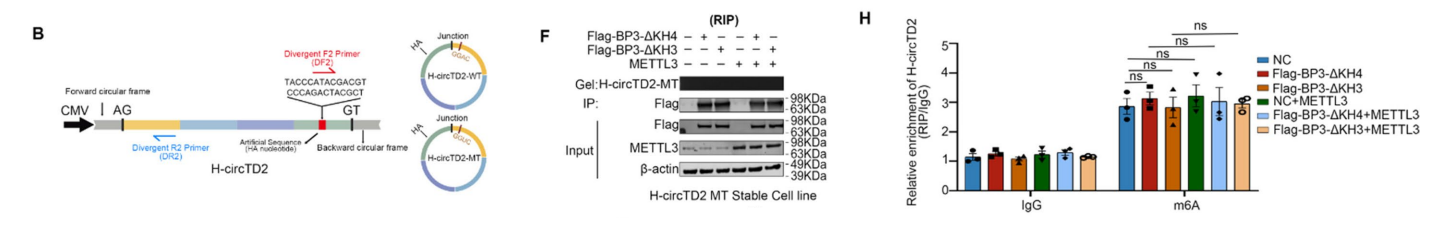
• MeRIPseq显示circHECTD2存在GG(m⁶A)C保守m⁶A位点,METTL3为核心甲基转移酶。
• 分子对接、EMSA、RIP证实,IGF2BP3通过KH3结构域直接结合circHECTD2的m⁶A位点。
• METTL3敲低降低circHECTD2的m⁶A水平,削弱IGF2BP3与circHECTD2的结合,加速circHECTD2降解。
• 回复实验表明,METTL3过表达可增强IGF2BP3对circHECTD2的稳定作用,m⁶A位点突变则使IGF2BP3无法调控circHECTD2。
3.4 circHECTD2作为ceRNA吸附miR4310和miR71575p
• 生物信息学预测与RAP、RIP、FISH共定位实验证实,circHECTD2直接结合并吸附miR4310与miR71575p。
• 过表达miR4310/71575p可显著抑制HNSCC细胞增殖、迁移与侵袭,发挥抑癌作用。
• 回复实验显示,miR4310/71575p可逆转circHECTD2的促癌效应,证实ceRNA调控关系。
3.5 miR4310/71575p直接靶向SMAD2并调控TGFβ通路
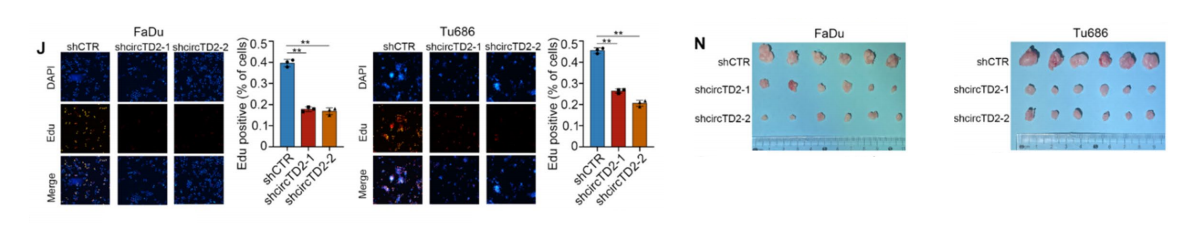
• RNA测序、KEGG与GSEA分析显示,IGF2BP3/circHECTD2主要调控TGFβ/SMAD2通路。
• 双荧光素酶实验证实,miR4310与miR71575p直接结合SMAD2 3'UTR并抑制其表达。
• HNSCC组织中miR4310/71575p低表达、SMAD2高表达,二者呈负相关;SMAD2高表达提示预后不良。
• 敲低SMAD2可逆转IGF2BP3/circHECTD2的促癌作用,过表达则恢复恶性表型。
3.6 完整调控轴的功能验证
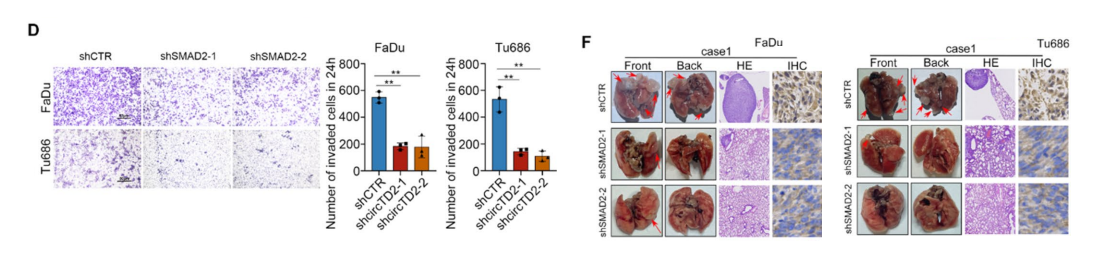
IGF2BP3→(m⁶A修饰)→circHECTD2→(海绵)→miR4310/71575p→(抑制解除)→SMAD2→(激活)→TGFβ通路→HNSCC增殖、侵袭、转移。
四、讨论
本研究首次揭示m⁶A修饰IGF2BP3circRNAceRNA轴在HNSCC中的关键促癌机制,主要创新点如下:1. 明确IGF2BP3的促癌功能:证实IGF2BP3在HNSCC中高表达并驱动增殖、侵袭与转移,是独立不良预后因子。
2. 发现新的circRNA分子:鉴定circHECTD2为HNSCC中关键促癌circRNA,受IGF2BP3以m⁶A依赖方式稳定。
3. 阐明分子互作机制:IGF2BP3通过KH3结构域结合METTL3介导的circHECTD2 m⁶A位点,增强circHECTD2稳定性。
4. 完善ceRNA调控网络:circHECTD2吸附miR4310/71575p,上调SMAD2激活TGFβ通路,推动HNSCC进展。
本研究存在一定局限:未开展体内靶向治疗实验;未系统评估干预策略的脱靶效应。未来可针对IGF2BP3、circHECTD2设计小分子抑制剂或核酸药物,推进临床转化。
五、结论
IGF2BP3在METTL3介导的m⁶A修饰下结合并稳定circHECTD2,circHECTD2通过ceRNA机制吸附miR4310和miR71575p,上调SMAD2表达并激活TGFβ通路,最终促进HNSCC增殖、侵袭与转移。
IGF2BP3、circHECTD2可作为HNSCC预后标志物与治疗靶点,为HNSCC的精准诊疗提供新方向。
六、总论
本文以临床高发病率、低生存率的头颈鳞癌为研究对象,聚焦 m⁶A 表观转录修饰与环状 RNA 调控两大前沿方向,围绕 m⁶A 读取蛋白 IGF2BP3 展开系统性研究。
首先通过临床大样本组织验证,确认 IGF2BP3 在头颈鳞癌中异常高表达,且与肿瘤恶性程度、淋巴结转移及患者不良预后密切相关;
体外细胞功能实验与体内动物模型共同证实,IGF2BP3 能够显著促进头颈鳞癌细胞增殖、克隆形成、侵袭迁移以及体内成瘤和远处转移,明确其致癌功能。
在机制层面,研究利用多组学高通量测序联合筛选,锁定具有 m⁶A 修饰的环状 RNA circHECTD2 为 IGF2BP3 的关键下游靶分子。
该研究证实,METTL3 介导的 m⁶A 修饰是 IGF2BP3 结合 circHECTD2 的前提条件,IGF2BP3 依靠 KH3 结构域识别并结合 circHECTD2 的 m⁶A 保守位点,抑制其降解、延长 RNA 半衰期,从而特异性上调 circHECTD2 表达,且不影响同源线性 mRNA。
后续 ceRNA 机制研究显示,定位于细胞质的 circHECTD2 可通过碱基互补配对,直接吸附并下调抑癌 miR-4310 与 miR-7157-5p 的生物学功能;而两种 miRNA 可直接靶向结合 SMAD2 mRNA 的 3'UTR 区域,抑制 SMAD2 表达。
circHECTD2 的海绵作用解除了 miRNA 对 SMAD2 的沉默抑制,上调 SMAD2 表达并激活 TGF-β 经典促转移通路,诱导肿瘤细胞上皮间质转化,最终加速头颈鳞癌恶性进展。
同时研究设计多组回复实验,从上下游双向验证了「IGF2BP3/circHECTD2/miR-4310&miR-7157-5p/SMAD2」信号轴的必要性与因果性。
整体而言,该研究完整阐明了 m⁶A 修饰介导 IGF2BP3 调控 circHECTD2 稳定性,进而通过 ceRNA 网络激活 TGF-β/SMAD2 通路的分子机制。
既完善了 m⁶A 表观修饰与环状 RNA 交叉调控的理论体系,也为头颈鳞癌提供了全新的预后评估分子标志物,以及 IGF2BP3、circHECTD2、SMAD2 等潜在精准治疗靶点,为后续临床靶向药物研发与联合治疗策略制定提供了坚实的实验依据与理论支撑


作者使用伯信生物明星产品MeRIP、RAP试剂盒进行分子调控机制研究。
伯信好物分享
MeRIP Kit
产品介绍:
RNA甲基化指发生在RNA分子上不同位置的甲基化修饰现象,属于转录后修饰,常见的甲基化修饰方式有6-甲基腺嘌呤(N6-methyladenosine,m6A)和5-甲基胞嘧啶(C5-methylcytidine,m5C)以及7-甲基鸟嘌呤(N7-methylguanosine,m7G)等。
RNA甲基化在调控基因表达、剪接、RNA编辑、RNA稳定性、控制mRNA寿命和降解、介导环状RNA翻译等方面可能扮演重要角色。利用甲基化RNA免疫共沉淀(Methylated RNA Immunoprecipitation,MeRIP)技术,可以对RNA转录后甲基化修饰图谱进行全面研究。
伯信 MeRIP Kit分为:
Bes5203-1(S) m6A MeRIP Kit 12T
Bes5203-1(N) m6A MeRIP Kit 40T
Bes5203-2(S) m6A MeRIP Kit(含m6A抗体) 12T
Bes5203-2(N) m6A MeRIP Kit(含m6A抗体) 40T
Bes5204-1(S) m5C MeRIP Kit 12T
Bes5204-1(N) m5C MeRIP Kit 40T
Bes5204-2(S) m5C MeRIP Kit(含m5C抗体) 12T
Bes5204-2(N) m5C MeRIP Kit(含m5C抗体) 40T
Bes5205-1(S) m7G MeRIP Kit 12T
Bes5205-1(N) m7G MeRIP Kit 40T
Bes5205-2(S) m7G MeRIP Kit(含m7G抗体) 12T
Bes5205-2(N) m7G MeRIP Kit(含m7G抗体) 40T
实验原理:
MeRIP利用m5C/m6A/m7G特异性抗体识别并结合mRNA上的m5C/m6A/m7G甲基化修饰位点,以RNA免疫共沉淀方法富集甲基化修饰片段,同时,结合高通量测序与qPCR,在全转录组范围内研究发生m5C/m6A/m7G甲基化修饰的RNA区域,及其对基因表达的调控作用。
技术流程:
结果实例:
产品优势:
1. 快速省时
2. 稳定可靠
3. 配备完整
RAP Kit
产品介绍
RNA 反义纯化技术(RNA Antisense Purification,RAP)用于研究RNA与RNA、RNA与蛋白质之间的相互作用。根据研究对象不同,RAP技术结合了高通量测序(RAP-Seq)和质谱技术(RAP-MS),分别研究与目标RNA互作的RNA和蛋白质。
伯信 RAP Kit分为:
Bes5103-1(S) RAP-RNA kit 12T
Bes5103-1(N) RAP-RNA kit 30T
Bes5103-2(S) RAP-Protein kit 12T
Bes5103-2(N) RAP-Protein kit 30T
Bes5103-3(S) RAP-RNA、protein kit 12T
Bes5103-3(N) RAP-RNA、protein kit 30T
实验原理:
RAP技术通过设计生物素探针组拉取目标RNA,使与其共同作用的RNA或蛋白质(RBPs)富集在磁珠上并被洗脱。最后,通过高通量测序得到该调控RNA转录调控的下游靶基因,同时,也可以通过Western Blot验证RBPs,或通过MS鉴定未知蛋白。
技术流程:
结果实例:
产品优势:
1. 伯信独立研发,具有自主知识产权。
2. 灵敏度高,稳定性好。
3. 检测方法领先,结果准确、重复性好。




