CircROR1 binds HNRNPL to regulate FOXO4 pre-mRNA splicing, promoting cutaneous melanoma metastasis and serving as a therapeutic target via RNAi-loaded PEG-LNPs
(IF=33.8990)《Molecular Cancer》
摘要
皮肤黑色素瘤(cutaneous melanoma, CM)恶性程度高、易早期转移且对免疫治疗易产生耐药,亟需新的分子靶点与治疗策略。
环状 RNA(circRNA)可通过结合 RNA 结合蛋白调控 mRNA 可变剪接,在肿瘤进展中发挥关键作用。
本研究旨在鉴定黑色素瘤中异常表达的 circRNA,并阐明其调控肿瘤转移的分子机制,同时开发靶向纳米药物用于治疗。
通过芯片筛选与临床样本验证,发现 circROR1(hsa_circ_0000082) 在转移性黑色素瘤中显著高表达,且与肿瘤转移及不良预后正相关。
功能实验表明,circROR1 在体外促进黑色素瘤细胞增殖、迁移、侵袭与上皮-间质转化(EMT)并抑制凋亡;在体内加速肿瘤生长并促进肺定植转移,同时通过下调 PD-L1 介导抗 PD-L1 免疫治疗耐药。
机制上,RNA pull-down、质谱及 RIP 实验证实 circROR1 直接结合剪接因子 HNRNPL,增强其蛋白稳定性并抑制核转位,进而调控 FOXO4 前体 mRNA 可变剪接,使抑癌亚型 FOXO4α 减少、促癌亚型 FOXO4ζ 增加。
回复实验证实,过表达 FOXO4α 可逆转 circROR1 的促转移效应。在此基础上,本研究构建 叶酸修饰 PEG 化脂质纳米颗粒 FA-PEG(si-circ),实现对 circROR1 的高效、稳定、靶向沉默。
该纳米药物在体内显著抑制黑色素瘤肺转移,生物相容性好、安全性高。
综上,circROR1/HNRNPL/FOXO4 剪接轴是驱动黑色素瘤转移的关键通路,circROR1 可作为转移性黑色素瘤的诊断标志物与治疗靶点,FA-PEG(si-circ) 为晚期黑色素瘤提供了具有临床转化前景的新型靶向治疗策略。
一、引言
皮肤黑色素瘤是高度恶性的皮肤肿瘤,具有早期转移、预后差、五年生存率低等特点。尽管靶向治疗与免疫检查点治疗取得进展,但耐药与远处转移仍是治疗失败的主要原因。
因此,揭示黑色素瘤转移的核心分子机制、发掘新型诊疗靶点具有重要临床价值。环状 RNA(circRNA)由前体 mRNA 反向剪接形成,结构稳定、组织特异性强,可作为分子海绵、调控转录、影响 mRNA 剪接等。
近年来研究表明,circRNA 通过结合剪接因子调控下游基因可变剪接,成为肿瘤转移调控的新范式。然而,circRNA-RBP-剪接轴在黑色素瘤中的作用仍不明确。
本团队前期发现 circROR1 在黑色素瘤中异常高表达,但其功能、机制及治疗价值尚未阐明。
据此提出科学假说:circROR1 可能通过结合剪接因子 HNRNPL 调控 FOXO4 剪接,进而促进黑色素瘤侵袭转移。本研究围绕该假说展开系统研究,旨在为黑色素瘤提供新机制、新标志物与新疗法。
二、材料与方法
2.1 临床组织样本与细胞:收集黑色素瘤组织、癌旁组织及痣组织;细胞株包括 HEM、WM35、WM451、A375、A2058、B16 及 HaCaT。
2.2 分子生物学实验:qRT-PCR、RNase R 处理、放线菌素 D 稳定性检测、核质分离、FISH、RNA pull-down、质谱、RIP、Western blot。
2.3 细胞功能实验:CCK-8、克隆形成、划痕愈合、Transwell 迁移与侵袭、流式细胞术凋亡检测。
2.4 动物模型:C57BL/6 小鼠皮下移植瘤模型、尾静脉肺定植模型;裸鼠 Luc-A375 肺转移模型与活体成像。
2.5 纳米药物制备与评价:微流控制备 FA-PEG(si-circ);凝胶阻滞、TEM、血清稳定性、细胞摄取、活体分布、组织病理学检测。
2.6 生物信息学与统计分析:差异表达分析、GO/Reactome 富集、RBPmap 预测、TCGA/GEO 数据集分析;统计学采用 t 检验、ANOVA 等,P<0.05 为差异具有显著性。
三、结果
3.1 circROR1 在转移性黑色素瘤中高表达且结构稳定
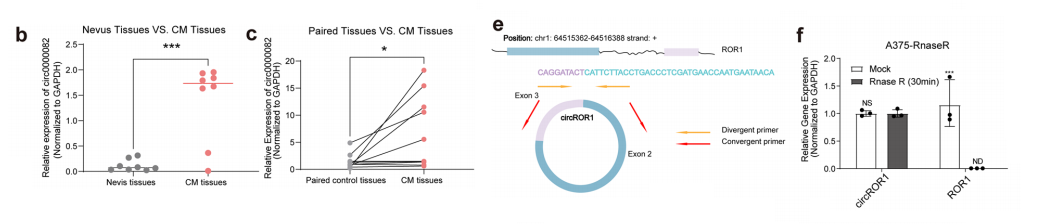 芯片筛选显示 circROR1 在高转移黑色素瘤细胞中显著上调。临床样本证实,circROR1 在黑色素瘤组织中高于正常组织与痣组织,转移灶显著高于原发灶,与 AJCC 分期及转移状态显著相关。
芯片筛选显示 circROR1 在高转移黑色素瘤细胞中显著上调。临床样本证实,circROR1 在黑色素瘤组织中高于正常组织与痣组织,转移灶显著高于原发灶,与 AJCC 分期及转移状态显著相关。
circROR1 由 ROR1 基因 2、3 号外显子反向剪接形成,抗 RNase R 降解、半衰期长,定位于细胞核与细胞质,符合剪接调控分子的定位特征。
3.2 circROR1 促进黑色素瘤增殖、侵袭、EMT 并介导免疫耐药
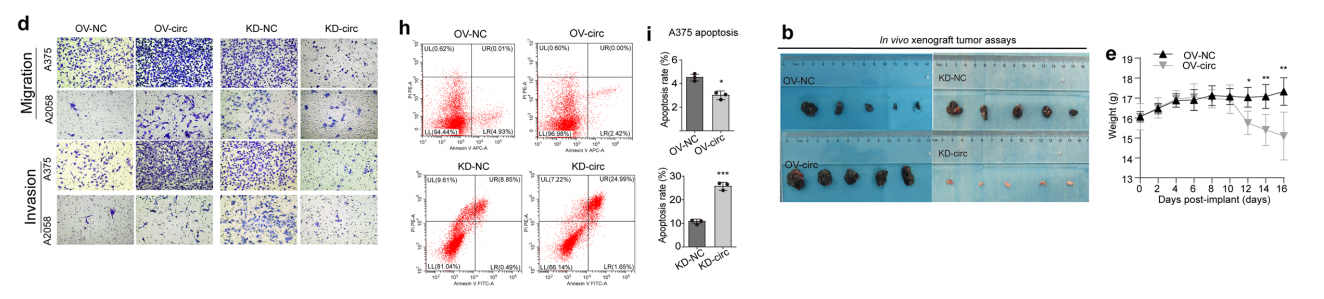 过表达 circROR1 可促进细胞增殖、克隆形成、迁移与侵袭,激活 EMT(N-cadherin、Vimentin、Snail 上调,E-cadherin 下调),抑制凋亡;敲低则表型逆转。
过表达 circROR1 可促进细胞增殖、克隆形成、迁移与侵袭,激活 EMT(N-cadherin、Vimentin、Snail 上调,E-cadherin 下调),抑制凋亡;敲低则表型逆转。
体内实验显示,circROR1 促进皮下肿瘤生长与肺转移结节形成。同时,circROR1 下调 PD-L1 表达,降低黑色素瘤对 PD-L1 抗体治疗的敏感性,介导免疫耐药。
3.3 circROR1 直接结合并调控 HNRNPL 表达与核转位
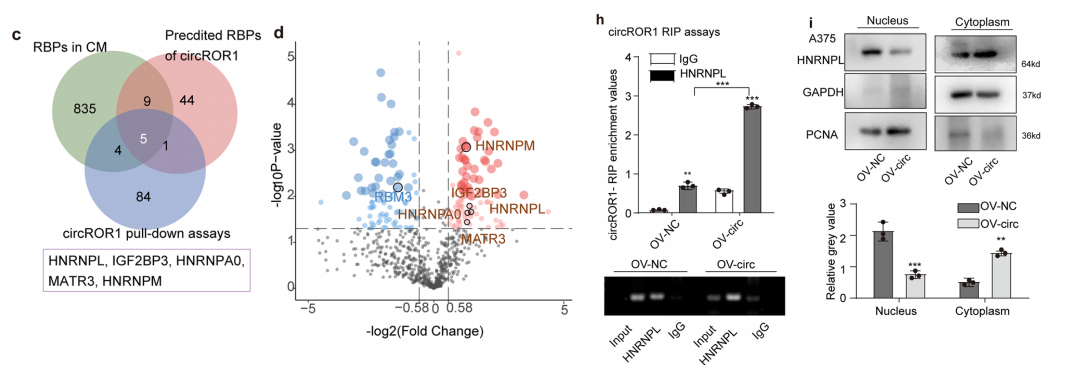 RNA pull-down 联合质谱筛选到剪接因子 HNRNPL。RIP 实验证实二者直接结合。circROR1 可增强 HNRNPL 蛋白稳定性,并将其滞留于细胞质,减少核内分布。
RNA pull-down 联合质谱筛选到剪接因子 HNRNPL。RIP 实验证实二者直接结合。circROR1 可增强 HNRNPL 蛋白稳定性,并将其滞留于细胞质,减少核内分布。
临床组织中 circROR1 与 HNRNPL 表达呈正相关。
3.4 circROR1/HNRNPL 调控 FOXO4 前体 mRNA 可变剪接
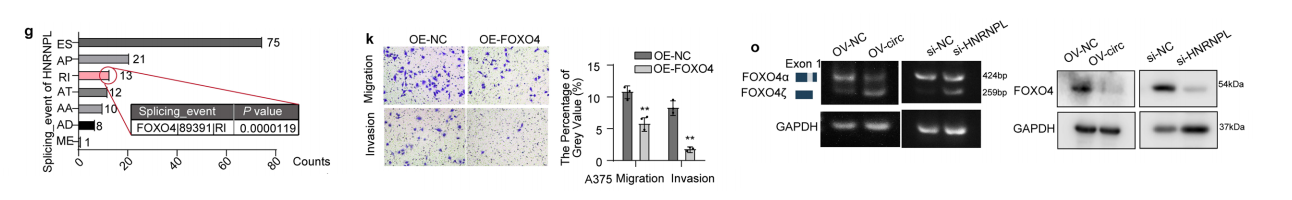 生物信息学与验证表明FOXO4 是 HNRNPL 的关键剪接底物。FOXO4 存在两种主要亚型:FOXO4α(全长、抑癌)与 FOXO4ζ(内含子剪切、促癌)。
生物信息学与验证表明FOXO4 是 HNRNPL 的关键剪接底物。FOXO4 存在两种主要亚型:FOXO4α(全长、抑癌)与 FOXO4ζ(内含子剪切、促癌)。
circROR1 过表达或 HNRNPL 敲低均导致:• FOXO4α 减少、FOXO4ζ 增加
• FOXO4 总蛋白水平下降回复实验显示,FOXO4α 过表达可逆转 circROR1 诱导的侵袭与 EMT,证实 FOXO4 为关键效应分子。
3.5 FA-PEG(si-circ) 纳米药物靶向抑制黑色素瘤转移
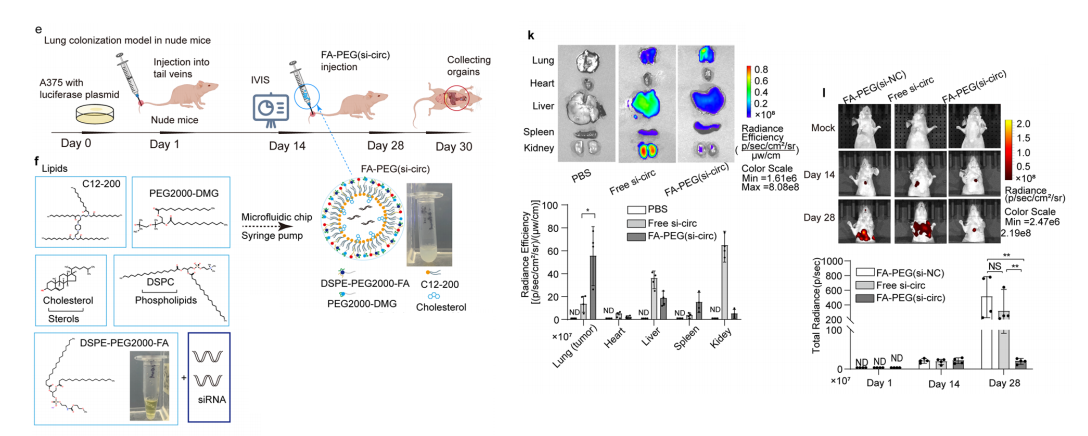 构建叶酸靶向纳米递送系统 FA-PEG(si-circ),粒径均一、包载效率高、血清稳定性强、肿瘤靶向性好。
构建叶酸靶向纳米递送系统 FA-PEG(si-circ),粒径均一、包载效率高、血清稳定性强、肿瘤靶向性好。
体外可高效沉默 circROR1 并抑制细胞恶性表型;体内可显著减少肺转移结节、降低活体荧光信号,对主要脏器无明显损伤,安全性良好。
此外,circROR1 在膀胱癌、结直肠癌、舌鳞癌等多种肿瘤中高表达,提示该策略具有泛癌治疗潜力。
四、讨论
本研究首次系统揭示 circROR1/HNRNPL/FOXO4 可变剪接轴在皮肤黑色素瘤转移中的关键驱动作用,并完成从机制解析到靶向纳米药物的完整转化链条。
首先,本研究明确 circROR1 是黑色素瘤的促癌 circRNA,其高表达与转移、免疫耐药密切相关,可作为独立预后标志物。
其次,本研究阐明了全新分子机制:circROR1 作为分子海绵结合 HNRNPL,调控其核质分布与蛋白稳定性,进而重编程 FOXO4 剪接,使抑癌亚型减少、促癌表型增强。
该机制将 circRNA、剪接因子、mRNA 可变剪接与肿瘤转移有机串联,丰富了非编码 RNA 调控肿瘤恶性进展的理论体系。
同时,本研究发现 circROR1 下调 PD-L1 并介导免疫耐药,提示其可作为联合免疫治疗的预测标志物与增敏靶点,为克服耐药提供新思路。
在转化层面,本研究构建的 FA-PEG(si-circ) 纳米药物具备靶向富集、高效沉默、稳定安全等优势,在体内显著抑制肺转移,为晚期黑色素瘤提供了可转化的新型 RNAi 治疗策略。
本研究仍存在一定局限:未深入解析 HNRNPL 与 FOXO4 前体 mRNA 的精确结合位点;FOXO4ζ 的具体功能有待进一步阐明;动物模型以实验性转移为主,未来可开展自发转移模型与临床前大动物验证。
综上,circROR1 是黑色素瘤转移的关键驱动因子与治疗靶点,circROR1/HNRNPL/FOXO4 轴可为黑色素瘤机制研究与精准干预提供全新方向,靶向 circROR1 的纳米疗法有望成为转移性黑色素瘤的重要治疗手段。
五、结论
1,circROR1 在转移性皮肤黑色素瘤中特异性高表达,是促进肿瘤增殖、EMT、远处转移及免疫耐药的致癌环状 RNA。
2. 分子机制:circROR1 直接结合剪接因子 HNRNPL,抑制其核转位并增强稳定性,进而调控 FOXO4 前体 mRNA 可变剪接,降低抑癌亚型 FOXO4α 表达,最终驱动肿瘤转移。
3. 治疗价值:叶酸靶向纳米药物 FA-PEG(si-circ) 可高效、安全地沉默 circROR1,显著抑制黑色素瘤肺定植,是极具前景的抗转移新型疗法。
4. circROR1 可作为皮肤黑色素瘤转移诊断标志物、预后评估指标与精准治疗靶点。


作者使用伯信生物明星产品RNA pulldown、RIP试剂盒进行分子调控机制研究。
RNA pulldown
产品介绍:
蛋白质与RNA的相互作用是许多细胞生物学过程的核心,如蛋白质合成、mRNA 组装、病毒复制、细胞发育调控等,研究它们之间相互作用的分子机制对理解这些生物学过程非常重要。
RNA pulldown技术通过体外转录标记生物素的RNA探针耦联链霉亲和素标记的磁珠,实现了对RNA结合蛋白质(RBPs)的高效富集和鉴定。
伯信 RNA pulldown Kit分为:
Bes5102(S) RNA pulldown kit 12T
Bes5102(M) RNA pulldown kit 24T
Bes5102(N) RNA pulldown kit 40T
实验原理:
针对目标区域设计生物素标记的特异性RNA探针偶联磁珠,并与细胞蛋白提取物孵育,蛋白分子与RNA探针特异性结合,经洗脱,得到目的RNA探针-蛋白质复合物。最后采用Western Blot或质谱鉴定蛋白质类型。
技术流程:
结果实例:
产品优势:
1. 自主品牌:拥有自主知识产权专利。
2. 高品质,稳定性好。
3. 精准:特异性高,背景少。
4. 易用:操作简单,容易上手。
5. 快速省时:全部实验只需3小时。
RIP试剂盒
产品介绍:
RNA Immunoprecipitation(RIP)是研究细胞内RNA与蛋白质结合的技术,是了解转录后调控网络动态过程的有力工具,可应用于miRNA调控靶点、RNA 与 RBPs(RNA结合蛋白)互作等研究。
伯信 RIP Kit分为:
Bes5101(S) RIP Kit 12T
Bes5101(M) RIP Kit 24T
Bes5101(N) RIP Kit 40T
实验原理:
RIP技术运用针对目标蛋白的抗体免疫沉淀相应的RNA-蛋白复合物,并纯化与蛋白结合的RNA。最后,结合基因特异性分析技术(PCR、qRT-PCR)或高通量分析技术(高通量测序、基因芯片),分析结合在复合物上的RNA类型及数量。
技术流程:
结果实例:
产品优势:
1. 伯信独立研发。
2. 提供优化的磁珠,适于免疫沉淀RNA-蛋白复合物。
3. 高品质,稳定性好,
4. 结果准确,重复性好。
5. 操作简单,快速省时。




